- 장내 미생물 및 TMAO에 의한 신장 섬유화 -
[연구필요성]
급성신손상은 급격한 신장 기능의 저하를 특징으로 하는 임상 증후군으로 환자의 동반질환 및 중증도에 따라 입원환자의 1-50%에서 발생하는 흔한 합병증이며, 사망률이 6-60%에 달하는 중요한 질환이다. 콩팥병 환자의 예후를 개선하기 위해서는 급성신손상 이후 만성콩팥병으로의 전환을 예방하고 적절히 치료하는 것이 매우 중요하나 아직 병태생리학적 요인과 치료방법에 대한 연구가 부족하다. 장내 미생물과 그 대사산물은 전신 염증과 콩팥병의 예후에 영향을 미칠 수 있을 것으로 기대된다. 연구자는 급성콩팥병 동물 및 세포모델과 중환자실 코호트의 인체자원을 활용하여 급성콩팥병의 예후와 관련된 대사체를 찾고, 항생제를 이용하여 장내 미생물 관련 대사체 생성을 감소시켜 신장섬유화를 완화시키며, 대사체에 의한 신장섬유화 발생을 매개하는 산화성 손상의 기전적 역할을 규명하고자 연구를 수행하였다.
[연구성과/기대효과]
본 연구에서 TMAO 대사체는 중환자실에서 지속성 신대체요법 치료를 시행받는 환자에서 3개월째 콩팥(신장)기능 악화와 유의한 관련성이 확인되었다. TMAO는 신장 섬유화 세포 및 동물모델에서 산화성 손상, 조직 염증, 세포사멸, 세포주기 정지 및 섬유화 반응을 증가시켰으며 항생제를 통한 장내 미생물 조절을 통해 TMAO 생성을 억제하거나 활성산소 생성인자 억제제 (NADPH oxidase 2 inhibitor, NOX2i)를 처리하여 산화성 손상을 억제하였을 때 신장 세포 및 조직의 손상, 염증 반응, 세포사멸 및 신장 섬유화가 호전되었다. 신장질환 특이적인 치료약제가 부족한 상황에서 이번 연구는 급성신손상 이후 만성콩팥병으로 진행을 매개하는 TMAO 대사체와 이를 통해 유도되는 산화성 손상의 역할을 확인하고, 장내 미생물 조절이나 활성산소 생성인자 억제제 등 효과적인 치료 방법을 제안했다는 점에서 급성콩팥병 및 신장섬유화 기전 및 치료 연구에 중요한 진전으로 평가된다.
[본문]
서울대학교(총장 유홍림) 의과대학 이정표 교수 연구팀이 한국기초과학지원연구원 황금숙 박사-서울대병원 의학연구혁신센터 양승희 교수팀과의 공동연구를 통해 장내 미생물에 의해 생성되는 TMAO(Trimethylamine N-oxide) 및 이에 의한 산화성 손상이 급성신손상 이후 발생하는 만성콩팥병의 주요한 원인으로 작용하며 이를 효과적으로 조절하여 질병을 호전시킬 수 있음을 규명하였다. 범부처재생의료기술개발사업단의 지원을 받아 수행한 이번 연구성과는 신장학 연구 분야 최고 국제학술지인 ‘Kidney International’에 게재되었다.
* 논문명: Antibiotic-induced intestinal microbiota depletion can attenuate the acute kidney injury to chronic kidney disease transition via NADPH oxidase 2 and trimethylamine-N-oxide inhibition
급성신손상은 급격한 신장 기능의 저하를 특징으로 하는 임상 증후군으로 환자의 동반질환 및 중증도에 따라 입원환자의 1-50%에서 발생하는 흔한 합병증이며, 사망률이 6-60%에 달하는 중요한 질환이다. 통상적으로 발생 요인이 해결되면 급성신손상에서 가역적으로 회복할 수 있는 것으로 알려져 있으나, 일부 환자에서는 비가역적인 손상이 지속되어 만성콩팥병으로 진행한다.
콩팥병 환자의 예후를 개선하기 위해서는 급성신손상 이후 만성콩팥병으로의 전환을 예방하고 적절히 치료하는 것이 매우 중요하나 아직 그 병태생리학적 요인과 치료방법에 대한 연구가 부족하다. 장내 미생물과 그 대사체는 염증 반응 및 산화성 손상과 관련되어 심혈관질환의 발생과 악화에 관여할 수 있음이 알려져 있으며 콩팥병의 예후에도 유의한 영향을 미칠 수 있을 것으로 주목받고 있다.
연구자는 급성콩팥병 동물 및 세포모델과 중환자실 코호트의 인체자원을 활용하여 급성콩팥병의 예후와 관련된 대사체를 찾고, 항생제를 이용하여 대사체 생성을 감소시켜 신장섬유화를 완화시키며, 대사체에 의한 신장섬유화 발생을 매개하는 산화성 손상의 기전적 역할을 규명하고자 연구를 수행하였다.
급성신손상으로 지속성 신대체요법을 시행받은 환자의 혈장을 이용한 전향적 대사체 분석 결과 TMAO 농도의 상승이 3개월째 콩팥(신장)기능 악화와 유의한 관련성이 있음을 확인하였다.
TMAO를 신장세뇨관세포에 적용하였을 때 활성산소 (ROS, reactive oxygen species)의 증가와 함께 신장세포 섬유화 반응이 유도가 되는 것을 확인하였다. 이후 활성산소 생성인자 억제제 (NADPH oxidase 2 inhibitor, NOX2i)를 처리하였을 때 활성산소의 생성이 줄어들고 TMAO에 의한 세포의 섬유화, 세포 사멸, 염증반응을 억제하며 세포주기를 활성화시키는 효과를 확인하였다.
일측 신장동맥결찰을 통한 마우스 급성신손상-만성콩팥병 이행 모델에서 TMAO의 생성의 증가와 함께 신장조직의 손상, 산화성 손상, 조직 염증, 세포사멸 등이 유의하게 증가됨을 확인하였고, 4가지 광범위 항생제를 마우스에 투여하여 장내 미생물 변화를 유도하였을 때 TMAO 생성과 관련된 장내 미생물의 감소와 함께 TMAO의 농도 상승을 억제할 수 있었다.
장내 미생물 조절을 통한 TMAO 생성 억제는 신장조직의 손상, 산화성 손상, 조직 염증, 세포사멸 등의 반응을 유의하게 호전시켰으며, 활성산소 생성인자 억제제 (NADPH oxidase 2 inhibitor, NOX2i)를 처리하였을 때에도 신장 조직의 손상, 산화성 손상, 조직 염증, 세포사멸 및 신장 섬유화를 호전시킬 수 있음을 확인하였다.
이 연구의 공동 1저자인 서울특별시 보라매병원 이정환 교수는 “이번 연구는 장내 미생물에 의해 생성되는 TMAO 대사체가 급성콩팥병 이후 발생하는 만성콩팥병 및 신장섬유화의 주요한 원인이며 TMAO 및 이와 관련된 산화성 손상을 줄여서 콩팥병의 예후를 개선시킬 수 있음을 밝힌 것”이라며, “다양한 콩팥병에서 장내 미생물 조절이나 산화성 손상의 억제를 통해 난치성 콩팥병의 예방 및 치료 가능성을 제시할 수 있었다”고 연구의 의의를 설명했다. 신장질환 특이적인 치료약제가 부족한 상황에서 이번 연구는 급성신손상 이후 만성콩팥병으로 진행을 매개하는 TMAO 대사체와 이를 통해 유도되는 산화성 손상의 역할을 확인하고, 장내 미생물 조절이나 활성산소 생성인자 억제제 등 효과적인 치료 방법을 제안했다는 점에서 급성콩팥병 및 신장섬유화 기전 및 치료 연구에 중요한 진전으로 평가된다.
[연구결과]
Antibiotic-induced intestinal microbiota depletion can attenuate the acute kidney injury to chronic kidney disease transition via NADPH oxidase 2 and trimethylamine-N-oxide inhibition
Jeonghwan Lee, Jinhaeng Lee, Kyuhong Kim, Jiwon Lee, Youngae Jung, Jin Seong Hyeon, Areum Seo, Wencheng Jin, Boram Weon, Nayeon Shin, Sejoong Kim, Chun Soo Lim, Yon Su Kim, Jung Pyo Lee, Geum-Sook Hwang, Seung Hee Yang
(Kidney International, https://doi.org/10.1016/j.kint.2024.01.040)
중환자실에 입원하여 중증의 급성신손상으로 지속성 신대체요법 치료를 시행받은 152명의 환자를 대상으로 혈장내 59개 대사체의 농도를 분석하였다. 3개월째까지 생존하여 콩팥(신장)기능을 확인할 수 있었던 61명 환자의 신장기능 예후와 대사체간의 분석을 통해 TMAO의 농도 증가가 3개월째 신장기능 예후의 악화와 유의하게 관련됨을 확인하였다.
인체의 세뇨관세포를 일차배양한 후 TMAO를 처리하여 활성산소 (ROS, reactive oxygen species)가 유의하게 증가함을 확인하였다. 이후 활성산소 생성인자 억제제 (NADPH oxidase 2 inhibitor, NOX2i)를 처리하였을 때 활성산소 생성을 유의하게 줄여서 TMAO에 의한 세포의 섬유화, 세포 사멸, 염증반응을 억제하며 세포주기 정지를 다시 활성화시키는 효과를 확인하였다.
마우스 모델에서 일측 신장동맥결찰을 시행하여 허혈-재관류 손상을 통해 급성신손상-만성콩팥병 이행 모델을 구축하였다. 질환모델에서 TMAO의 생성의 증가와 함께 신장조직의 손상, 산화성 손상, 조직 염증, 세포사멸 등이 유의하게 악화됨이 확인되었다.
4가지 광범위 항생제 (neomycin, metronidazole, ampicillin, vancomycin)를 마우스에 투여하여 항생제를 통한 마우스의 장내 미생물 변화를 성공적으로 유도하였다. 이를 통해 TMAO 생성과 관련된 Desulfovibrio, Clostridium 등의 장내 미생물을 감소시켰으며 질환모델에서 TMAO의 농도 상승을 억제할 수 있음을 증명하였다.
장내 미생물 조절을 통한 TMAO 생성 억제는 신장조직의 손상, 산화성 손상, 조직 염증, 세포사멸 등의 반응을 유의하게 호전시켰다.
마우스 동물질환 모델에서 활성산소 생성인자 억제제 (NADPH oxidase 2 inhibitor, NOX2i)를 처리하였을 때 장내 미생물의 변화나 TMAO 농도의 변화 없이 신장 조직의 손상, 산화성 손상, 조직 염증, 세포사멸 및 신장 섬유화가 호전됨을 확인하였다.
이번 연구를 통해 TMAO가 급성신손상 이후 발생하는 만성콩팥병 발생의 주요한 원인 대사체임을 증명하였으며, TMAO에 의해 증가하는 산화성 손상이 주요한 병태생리학적 요인으로 작용하며 이를 효과적으로 억제하는 경우 급성신손상 이후 발생하는 만성콩팥병의 발생 및 신장섬유화를 효과적으로 치료할 수 있음을 증명하였다.
[용어설명]
- ○콩팥(신장)의 기능이 수시간에서 수일 사이에 급속도록 악화되는 질환
- ○혈청크레아티닌 수치의 상승이나 소변량의 감소 정도에 따라 1단계에서 3단계로 분류
- ○콩팥(신장)의 기능이 일주 이상에서 3개월 사이에 지속적으로 악화되는 질환
- ○콩팥(신장)의 기능이 3개월 이상 지속적되거나 콩팥손상의 증거(지표)가 3개월 이상 지속되는 질환
- ○음식으로 섭취한 콜린, L-카르니틴 등이 장내 미생물에 의해서 대사되어 생성되는 대사체
[그림설명]
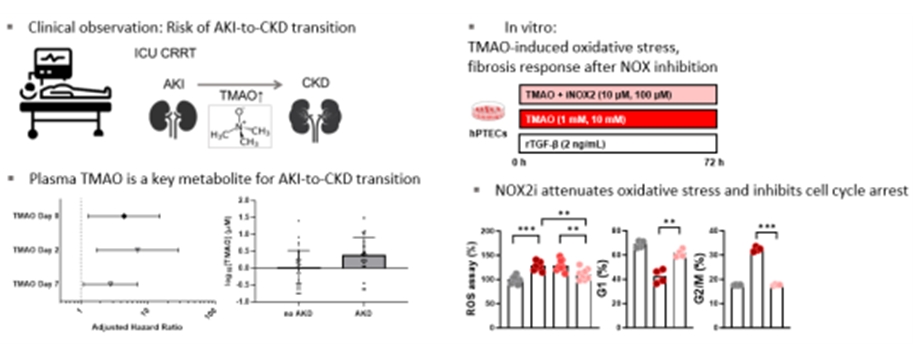
그림. 중환자실에서 지속성 신대체요법 치료를 시행받은 환자를 대상으로 혈장내 59개 대사체의 농도를 분석하고 환자의 3개월째 신기능 예후와의 관련성을 분석함. 3개월째 신장질환 예후의 악화와 TMAO 농도의 증가가 유의하게 관련성이 확인됨. 인체의 세뇨관세포를 일차배양한 후 TMAO를 처리하여 활성산소 (ROS, reactive oxygen species)가 유의하게 증가함. 이후 활성산소 생성인자 억제제 (NADPH oxidase 2 inhibitor, NOX2i)를 처리하였을 때 활성산소 생성이 유의하게 감소함을 확인함. 활성산소 생성인자 억제제는 TMAO에 의한 G2/M 세포주기 정지를 다시 활성화시키는 효과를 보여줌.
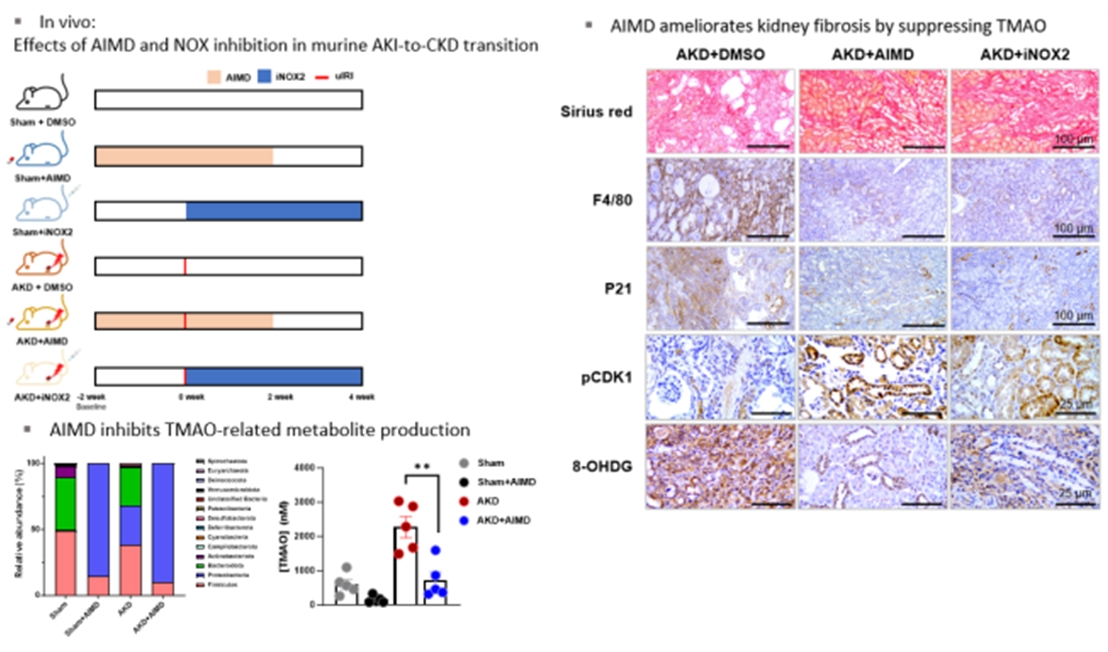
그림. 마우스 모델에서 일측 신장동맥결찰을 통한 허혈-재관류 손상을 통해 급성신손상-만성콩팥병 이행을 유도함. 질환모델에서 TMAO의 농도가 유의하게 증가함을 확인함. 항생제를 처리하여 장내 미생물의 유의한 변화를 유도하였으며 이를 통해 질환모델에서 TMAO의 증가를 효과적을 억제할 수 있었음. 항생제를 통한 장내 미생물의 조절은 신장조직에서의 섬유화, 염증반응, 세포사멸, 세포주기 정지, 산화성 손상을 모두 호전시켰으며, 이러한 효과는 활성산소 생성인자 억제제 (NADPH oxidase 2 inhibitor, NOX2i)를 사용하였을 때 장내 미생물의 변화나 TMAO 농도의 변화와 독립적으로 유도가 가능하였음.

