- 대사유전체 (metabologenomics) 방법론을 개발을 통한 옥사졸 함유 신규 생리활성 천연물 발굴 -
[연구필요성]
전통적인 천연물 연구에서는 무작위적 물질 탐색 전략이 주류를 이루고 있어, 구조적으로 어떤 물질을 발견할지 예측할 수 없고, 따라서 논리적인 신규 물질 탐색이 제한적이었다. 따라서 천연물 연구에 있어 이러한 임의성을 극복하고 발견하고자 하는 천연물을 표적하여 발굴하는 논리적 방법론 개발이 필요하다.
[연구성과/기대효과]
본 연구에서는 옥사졸 구조를 생합성하는 효소를 코드화한 유전자를 가진 미생물 균주를 선별하고. 미생물의 복잡한 추출물에서 분리, 정제 없이 표적한 옥사졸 함유 천연물 생산을 대사체적으로 확인하는 방법을 융한한 대사유전체적 방법론 (metabologenomic method)를 개발하였다. 이 방법을 활용하여 말단에 옥사졸을 가지면서 항균, 그리고 선택적이면서 유방암에 대해 선택적 활성이 뛰어난 물질들을 포함하여 5개의 신규 물질을 발굴하였다. 또한 옥사졸과 같은 헤테로사이클 모핵을 포함하는 천연물의 생산 여부를 동위원소 표지 없이 확인할 수 있는 방법을 제시하였다.
[본문]
서울대학교 약학대학 천연물과학연구소 오동찬 교수 연구팀은, 미생물의 이차대사물질의 생합성 유전자(genomics)와 대사체적 특성(metabolomics)에 대한 총체적인 이해를 결합한 metabologenomics 방법으로 말단에 옥사졸 모핵을 포함하는 천연물의 표적화된 발굴 기술을 개발하였다고 보고하였다. 해당 기술을 통해 말단에 옥사졸을 포함하는 5개의 신규 물질 lenzioxazole, permafroxazole, tenebriazine, 그리고 methyl-oxazolomycin A와 B를 발굴하였다. 말단에 옥사졸을 포함하면서 변형된 아미노산 구조를 가지는 tenebriazine은 병원성 진균 Candida albicans, Trichophyton rubrum, T. mentagrophytes에 대한 저해 활성을 나타냈고, methyl-oxazolomycin A와 B는 유방암에 대한 특이적이고 강한 억제 활성을 나타내었다.
본 연구결과는 세계 최정상급 화학 학술지인 독일 화학회지 (Angewandte Chemie International Edition, 피인용지수 16.6)에 “Discovery of Terminal Oxazole-Bearing Natural Products by a Targeted Metabologenomic Approach”라는 제목으로 게재되었다.
(https://doi.org/10.1002/anie.202402465, 공동 제1저자: 서울대학교 약학대학 박지윤 박사과정, 신연혁 박사, 황성훈 박사, 교신저자: 오동찬 교수)
미생물의 이차대사물질, 즉 천연물은 신약개발의 근간이 되어 왔다. 그러나, 전통적인 천연물 연구에서는 무작위적 물질 탐색 전략이 주류를 이루고 있어, 논리적인 신규 물질 탐색이 제한적이었다. 이를 해결하고자 서울대학교 약학대학 오동찬 교수(천연물과학연구소장) 연구실에서는 유전자적, 분광학적 시그니처를 이용해 특정 구조적 모핵을 포함하는 논리적인 신규 천연물의 발굴을 연구해왔다. 이를 통하여 우연한 발견에 의존하는 이전의 천연물 연구를 발굴하고자 하는 특정 구조적 모핵을 포함하는 천연물을 선택적이고 논리적으로 발굴하는 새로운 방향으로 발전시킬 필요성이 높다.
본 연구는 과학기술정보통신부 (Ministry of Science and ICT)의 중견연구자사업의 지원을 받아 수행되었다.
[연구결과]
Discovery of Terminal Oxazole-Bearing Natural Products by a Targeted Metabologenomic Approach
Jiyoon Park, Yern-Hyerk Shin, Sunghoon Hwang, Jungwoo Kim, Dong Hyun Moon, Ilnam Kang, Yoon-Joo Ko, Beomkoo Chung, Hyungsung Nam, Seokhee Kim, Kyuho Moon, Ki-Bong Oh, Jang-Cheon Cho, Sang Kook Lee, Dong-Chan Oh
(Angewandte Chemie International Edition, https://doi.org/10.1002/anie.202402465)
본 연구에서는 헤테로 고리 (heterocyclic) 화합물 중 하나인 옥사졸을 표적으로 하였고, 그 중에서도 말단에 위치한 옥사졸 화합물의 생합성 과정에 해당하는 폴리케티드 (polyketide)와 비리보솜 펩티드 (nonribosomal peptide)의 혼성체의 생합성 경로에 필수적인 사이클화 효소 (cyclase)를 암호화하는 유전자의 보존된 서열을 기반으로 프라이머를 제작하였다. 이에 옥사졸을 포함하는 물질을 생합성하는 잠재력을 가지는 균주들을 선별하였고, 모핵의 분광학적 특성을 이용하여 동위원소 표지 없이 배양 초기 단계에서 간단하게 실제로 옥사졸을 포함하는 물질이 생산되는지 확인하였다 (그림 1). 이후 옥사졸의 생합성과 관련된 필수 사이클화 효소를 코드화한 유전자를 가지면서 실제로 물질이 생산되는 균주들을 최종 선별하였고, 옥사졸을 가지는 기지 물질과 5종의 신규 물질들을 발굴하였다.
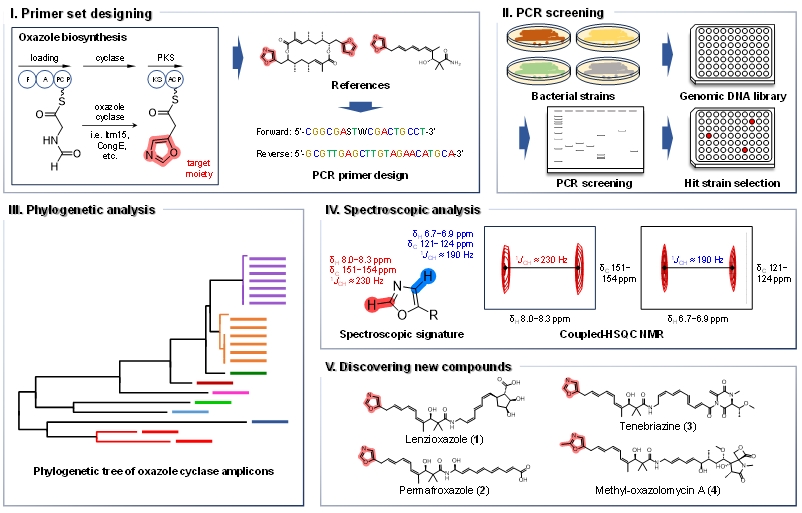
그림 1. Metabologenomics 방법을 활용한 옥사졸 포함 천연물의 발굴 과정
옥사졸의 생합성 중 폴리케티드 (polyketide)와 비리보솜 펩티드 (nonribosomal peptide) 하이브리드로 형성되는 경우 사이클화 효소는 formyl-glycyl을 기질로 사용하고 이 기질은 항상 물질의 생합성이 시작되는 loading module에서 형성이 되기 때문에 이 경우 옥사졸은 항상 물질이 처음 생합성되는 말단에 위치한다. 옥사졸 형성에 필수적인 사이클화 효소의 유전자의 보존되어 있는 서열을 표적으로 하여 프라이머를 디자인한 후 1,000개의 균주에 대해 polymerase chain reaction (PCR) 스크리닝을 하였다. 그 결과 16개의 균주에서 해당 효소를 가질 것으로 확인하였다. 디자인한 프라이머를 이용해 증폭된 amplicon을 계통분류학적으로 분석을 하였을 때 bootstrap score 90% 기준으로 9개의 clade로 구성된다. 기지물질과 신규물질들의 구조를 규명하여 계통수와 연관 지어보았을 때 옥사졸이 위치한 반대쪽 말단 부분에 구조적 다양성을 가짐을 규명하였고, 구조와 clade간 상관관계를 밝힐 수 있었다 (그림 2).
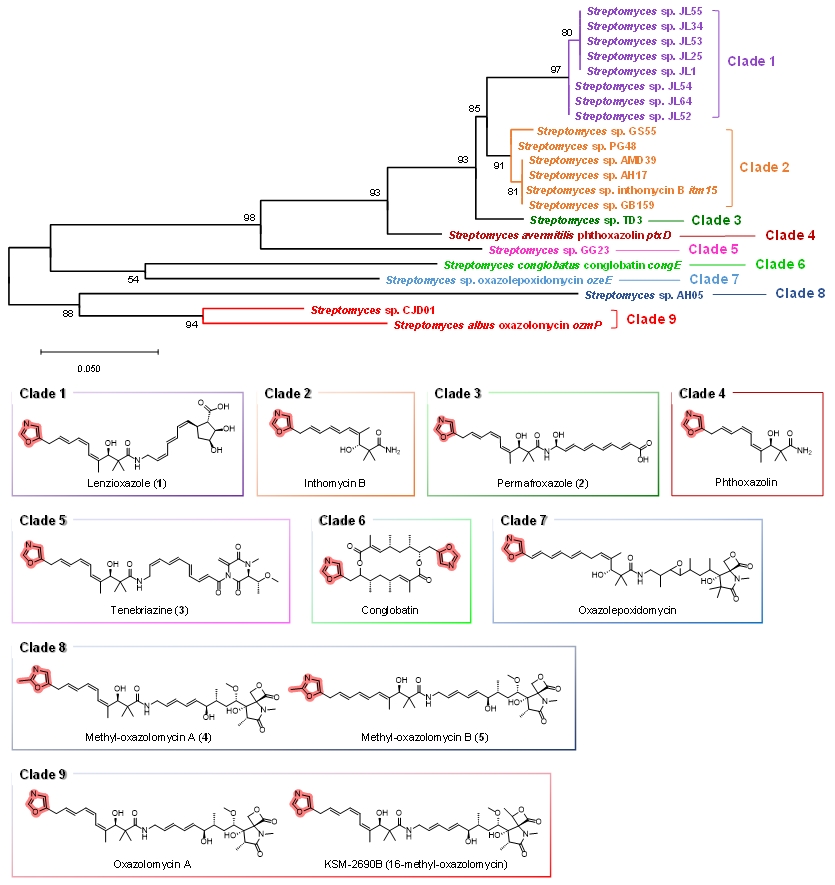
그림 2. 옥사졸을 생합성하는 사이클화 효소들의 계통분류학적 분석
옥사졸은 산소와 질소를 가지는 5원자고리의 헤테로고리화합물이다. 이 옥사졸은 구성하는 원자핵 주위의 전자상태에 따라 옥사졸을 구성하는 원자들은 핵자기공명 (NMR) 분석 시에 고유한 화학적 이동 (chemical shift) 값을 가진다 (그림 3). 옥사졸을 함유하는 기지물질 KSM-2690B의 생산균주 CJD1의 배양 추출물을 1H-13C coupled-HSQC NMR 실험을 수행하여 이 화학적 이동 값에서 1JCH를 측정하였고 옥사졸은 1번 위치에서 230 Hz, 2번 위치에서 190 Hz의 분광학적 시그니쳐를 가지는 것으로 규명하였다. 이 점을 이용하여 PCR 스크리닝하여 선별된 균주들의 배양 추출물을 대상으로 크로마토그래피법 등에 의한 분리, 정제 없이 옥사졸 함유 물질들의 생산 유무를 확인하는 방법을 확립하였다. 이는 동위원소 표지 등이 필요 없이 헤테로고리화합물을 혼합물에서 간편하게 확인할 수 있는 획기적인 방법이다.
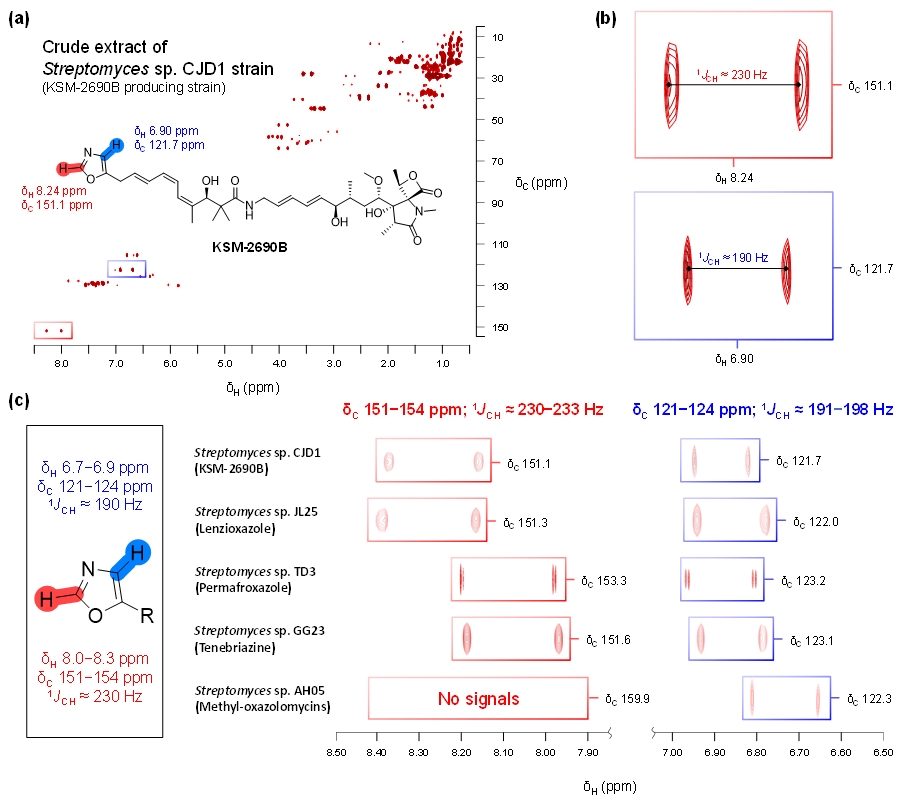
그림 3. 옥사졸을 구성하는 수소와 탄소의 화학적 이동값과 옥사졸의 1H-13C coupled-HSQC NMR 스펙트럼의 1JCH 분석
신규 물질 중 하나인 tenebriazine은 C. albicans, A. fumigatus, T. rubrum, T. mentagrophytes에 대한 항균활성을 가졌고, methyl-oxazolomycin A와 B는 MCF7, T-47D의 유방암 세포주에 대해 선택적으로 높은 저해 활성을 나타냈으며 다른 암세포주에서는 약한 활성을 나타내었다. 따라서 신규 옥사졸 포함 물질들의 약학적 응용성을 제시하였다.

